Как «Медисорб» доказывает, что его дженерики так же эффективны и безопасны, как оригинальные препараты?
Для этого проводят особый вид клинического исследования – исследование биоэквивалентности (или фармакокинетической эквивалентности) сравниваемых лекарственных препаратов.
Биоэквивалентность изучают на здоровых добровольцах после приема разовых доз оригинального препарата и дженерика. У добровольцев отбирают пробы крови через определенные промежутки времени для измерения концентрации действующих веществ и оценки скорости и степени их всасывания и выведения.
Аналитическая часть клинических исследований биоэквивалентности, то есть анализ проб добровольцев, проводится в специальных биоаналитических лабораториях.
Биоаналитические лаборатории оснащены современным высокочувствительным хроматографическим оборудованием, которое позволяет определять концентрации исследуемых соединений вплоть до 1*10-15 гр.
Разработка биоаналитической методики заключается в подборе оптимальных хроматографических условий для определения действующих веществ и их активных метаболитов в биологических жидкостях (плазма, кровь, моча и др.).
Согласно современным регуляторным требованиям каждая биоаналитическая методика подлежит полной валидации. Валидацией называют процесс экспериментального подтверждения того, что методика пригодна для конкретного исследования.
В рамках валидации оцениваются следующие параметры биоаналитической методики: селективность, линейность, нижний предел количественного определения (НПКО), эффект переноса, правильность, прецизионность, эффект матрицы и стабильность.
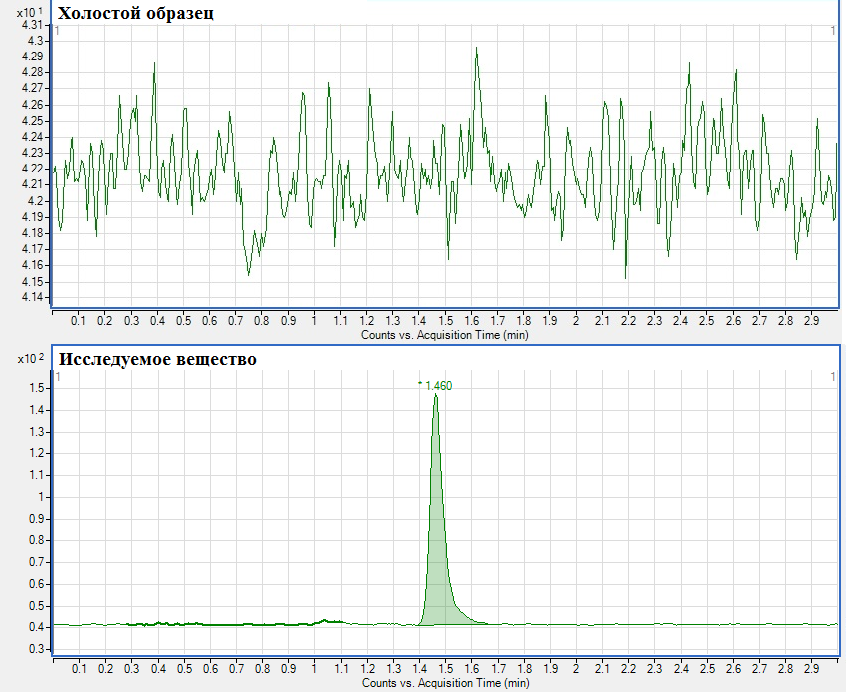
Селективность характеризует способность методики различать анализируемое вещество от мешающих анализу компонентов биологических образцов.
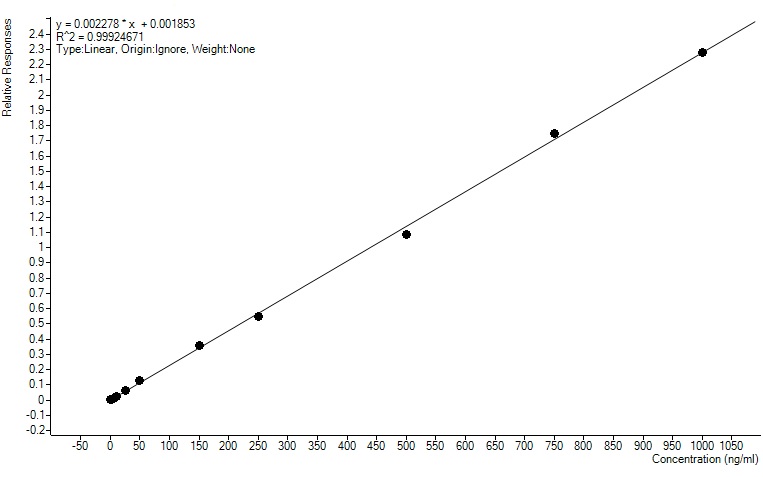
Линейность методики отражает зависимость сигнала детектора (площади хроматографического пика) от концентрации изучаемого соединения в пробе. Линейность изучают на модельных образцах, которые готовят путем добавления точного количества анализируемого вещества к холостой пробе той же ее разновидности, которая будет получена в исследовании (цельная кровь, плазма крови и т.д.).
Нижний предел количественного определения (НПКО) - наименьшее количество анализируемого вещества в пробе, которое поддаётся количественному определению.
Для минимизации риска переноса анализируемого вещества от пробы к пробе в процессе валидации оценивается эффект переноса, который определяют путем ввода холостых образцов после образцов с высокой концентрацией вещества.
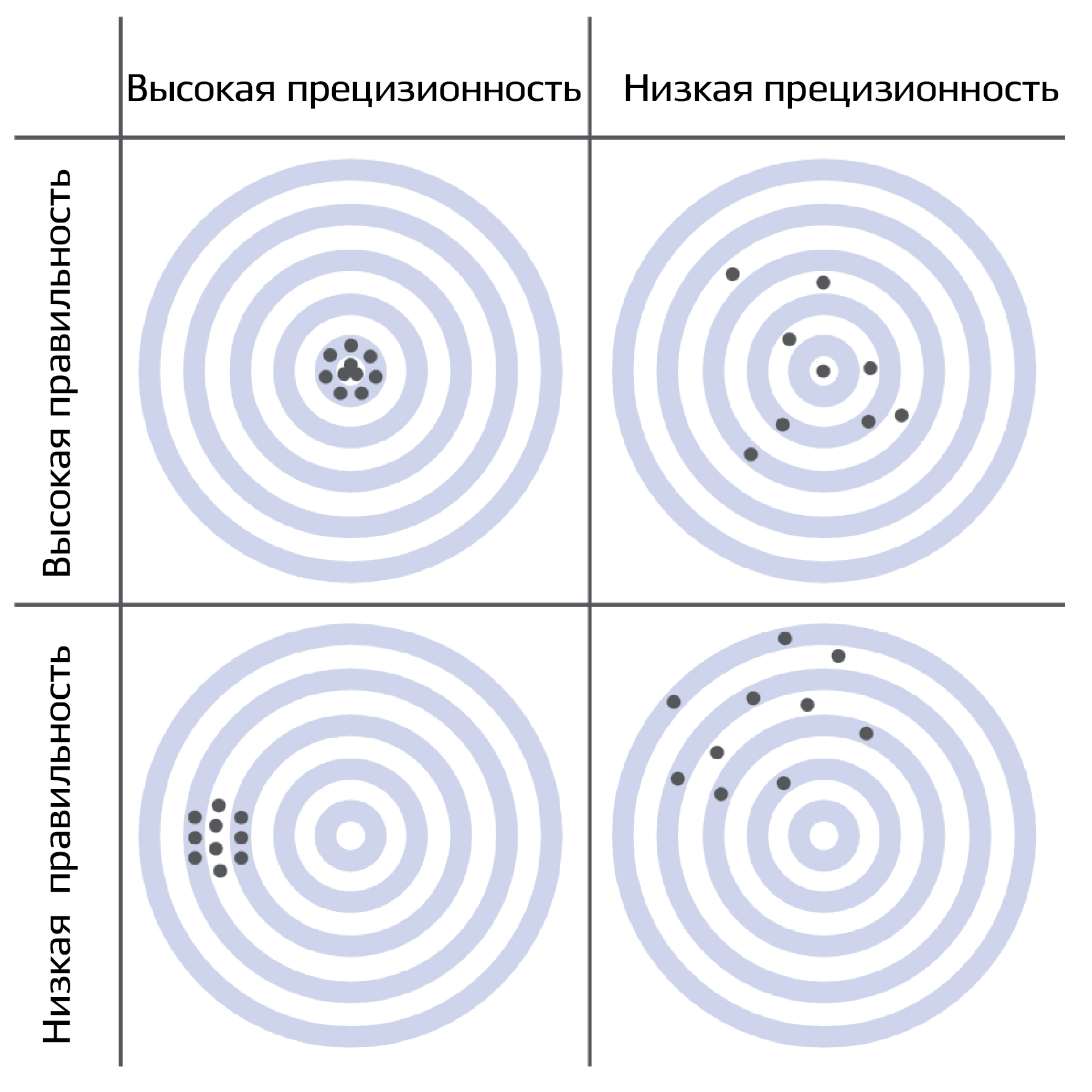
Правильность биоаналитической методики отражает близость полученных значений к истинным концентрациям исследуемого вещества.
Прецизионность методики - это степень близости результатов между повторными измерениями одной и той же пробы.
Оценка правильности и прецизионности проводится путем анализа модельных образцов (образцов контроля качества) с известной концентрацией соединения.

Эффект матрицы – это оценка влияния на результаты анализа мешающих компонентов биологических образцов. Эффект матрицы оценивают на «стандартной» плазме, а также на образцах гиперлипидемической плазмы и плазмы, полученной из крови, подвергшейся гемолизу).
Чтобы удостовериться, что каждый этап пробоподготовки и последующего анализа образцов, а также условия их хранения не повлияли на концентрацию анализируемого вещества, проводят исследование стабильности.
Проводят следующие испытания стабильности:
- стабильность растворов анализируемого вещества;
- стабильность соединения в биологическом образце в 3 циклах «замораживания – размораживания»;
- стабильность анализируемого вещества в биологическом образце при хранении при комнатной температуре;
- естественное хранение биологического образца, содержащего анализируемое вещество в замороженном виде;
- стабильность подвергшихся пробоподготовке образцов в устройстве для автоматического ввода пробы.
По итогам валидации оформляется Валидационный отчет.
Использование валидированных биоаналитических методик гарантирует получение точных результатов аналитической части клинического исследования и достоверное установление биоэквивалентности между оригинальным и воспроизведенным препаратом.




